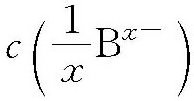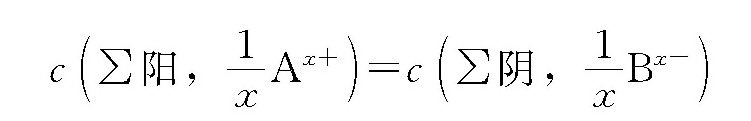凡能提供或接受1mol氢离子的物质的质量称为以氢离子为基本单元的摩尔质量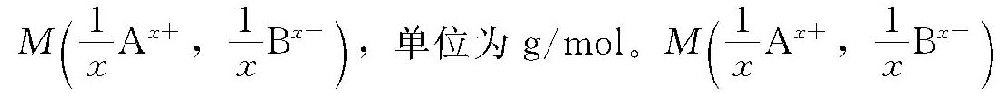 对计算以氢离子为基本单元的物质的量浓度不可缺少。
对计算以氢离子为基本单元的物质的量浓度不可缺少。
酸碱盐的H+摩尔质量必须根据化学反应式来确定,同一物质在不同反应式中可以有不同的H+摩尔质量。例如,H3PO4与NaOH反应,有以下三种方式:
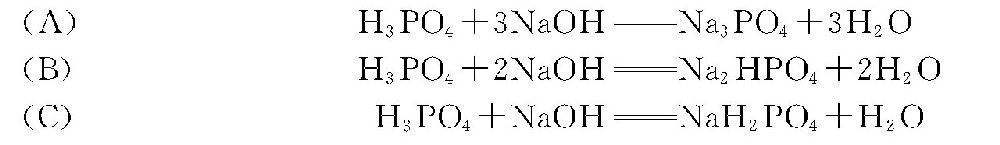
(1)酸的H+摩尔质量M![]() 的计算:
的计算:

![]() ,分别为3、2、1。H3PO4的摩尔质量M(H3PO4)为98g/mol。所以,(A)、(B)、(C)三式中H3PO4的H+摩尔质量分别是:
,分别为3、2、1。H3PO4的摩尔质量M(H3PO4)为98g/mol。所以,(A)、(B)、(C)三式中H3PO4的H+摩尔质量分别是:
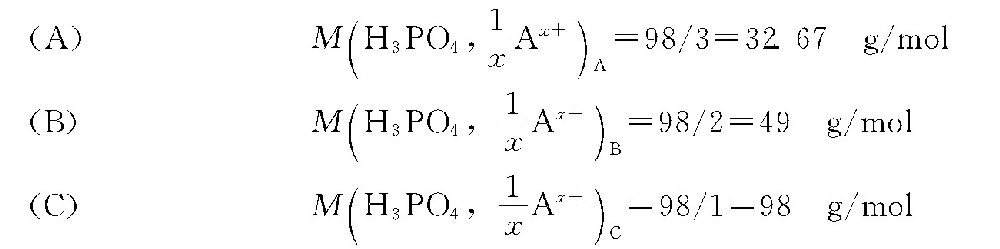
(2)碱的H+摩尔质量
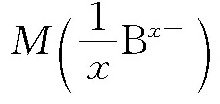 的计算:
的计算:

NaOH的摩尔质量M(NaOH)为40g/mol。所以三式中NaOH的H+摩尔质量均为:
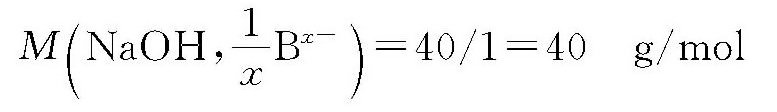

在水溶液中溶质B的以氢离子为基本单元的物质的量浓度,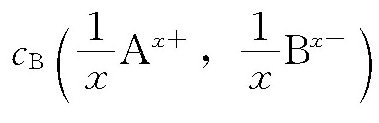 相当于当量浓度,与物质的量浓度cB有以下关系;
相当于当量浓度,与物质的量浓度cB有以下关系;
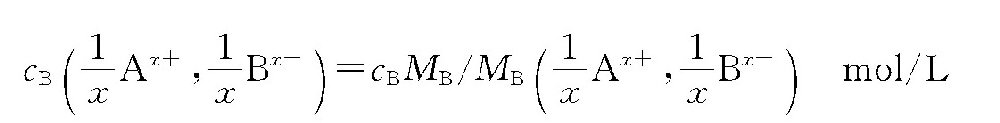
式中 MB———B溶质的摩尔质量,g/mol;

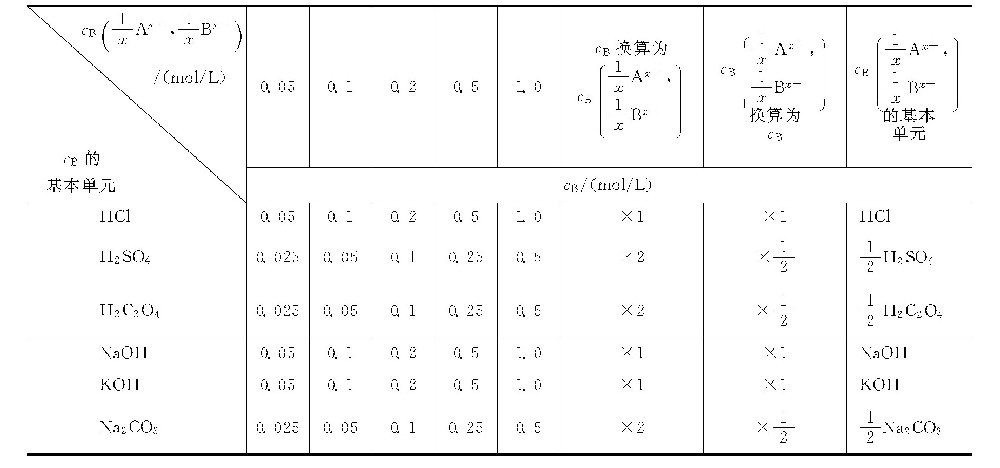
按上式,分析化学中常用的一些化学品的 的关系如下。
的关系如下。
(1)酸碱滴定
(2)氧化还原滴定