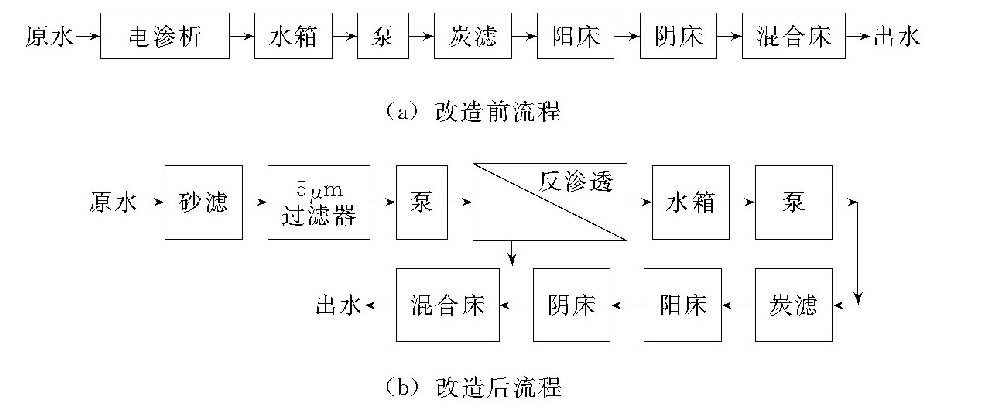
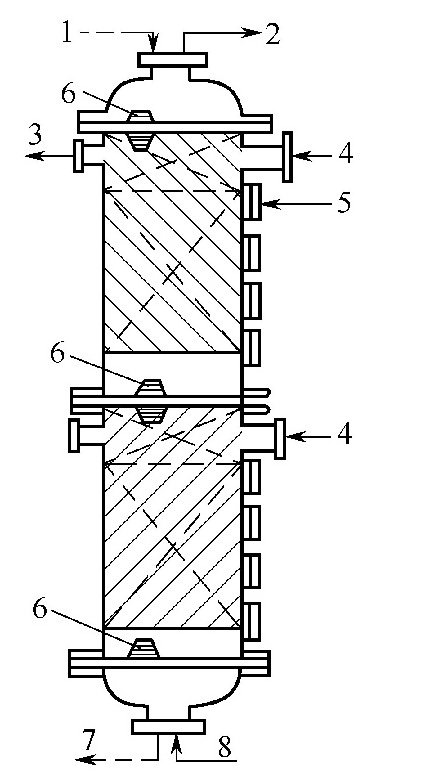
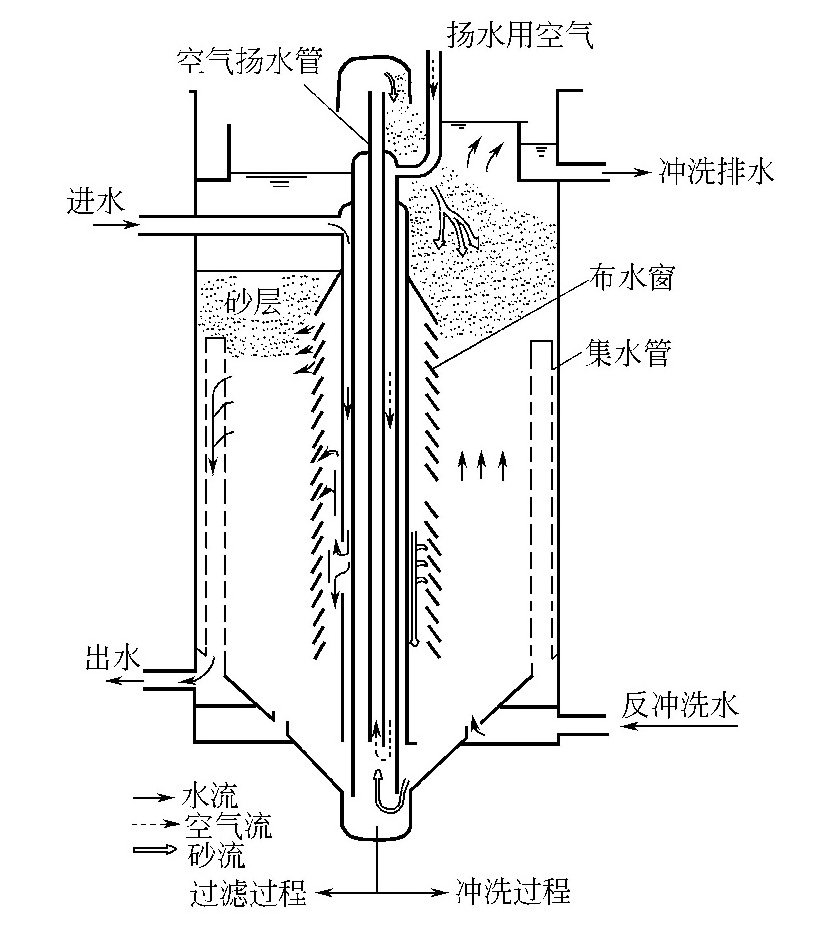
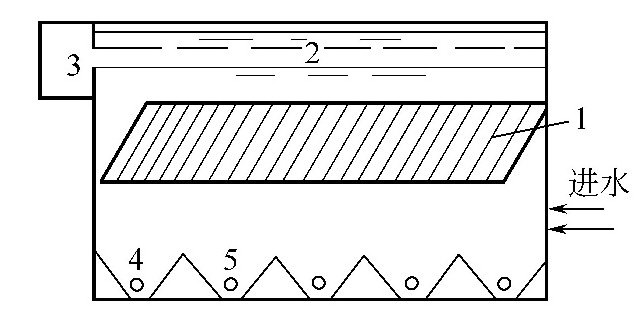
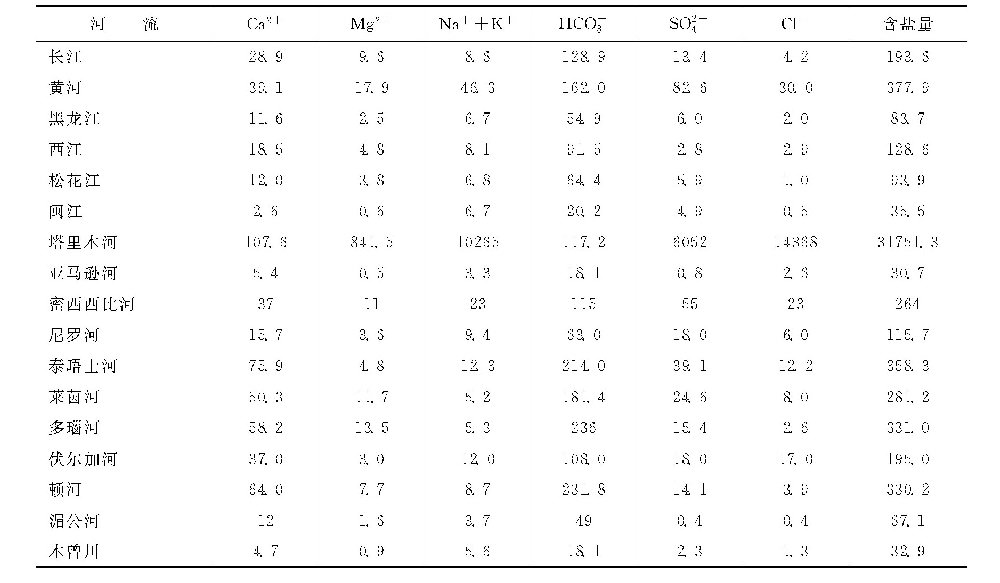
在离子交换过程中,被吸附离子在树脂中是按吸附能力大小分层吸附的。现以阳离子交换树脂说明分层吸附原理。天然水中不会只含单纯一种阳离子,通常都含有多种阳离子。为了说明问题,以含有Fe3+、Ca2+和Na+的水通过刚再生好的H型离子交换树脂为例,其分层吸附原理见下图。
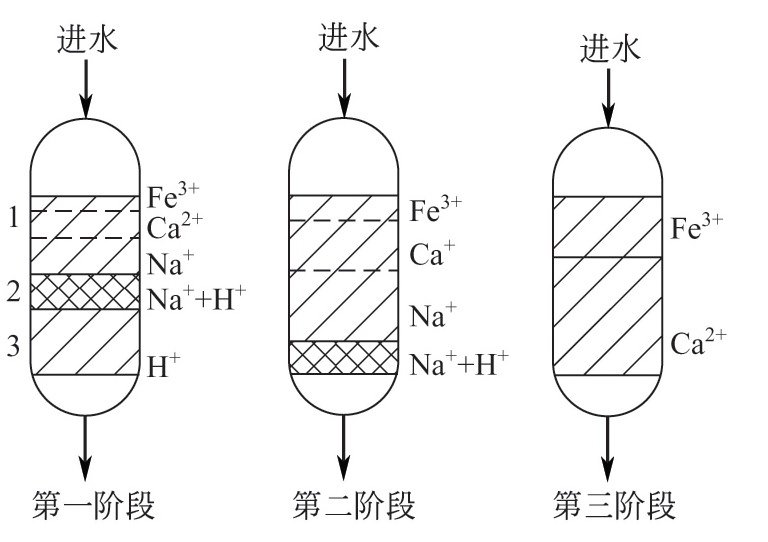
分层吸附原理:1—失效层;2—工作层;3—保护层
进水的初期,由于交换树脂是H型,故水中各种阳离子都与树脂上的H+相交换。但因各种阳离子选择性的不同,交换树脂吸附的离子在树脂层中有分层现象。即依据离子被树脂吸附能力的大小,自上而下依次被吸附的顺序为Fe3+、Ca2+、Na+。
第一阶段当交换床不断进水时,由于Fe3+比Ca2+和Na+更易被吸附,于是进水中的Fe3+可与已吸附了Ca2+的树脂层进行交换,Ca2+被Fe3+置换下来,使吸附Fe3+的交换层不断扩大;而被置换下来的Ca2+会连同进水中的Ca2+一起,又进入已吸附了Na+的树脂层,将Na+置换下来,使吸附Ca2+的交换层不断扩大和下移。
同理,吸附Na+的交换层也会不断扩大和下移。
在吸附Na+的树脂层下面,有一层树脂层是Na+和H型树脂进行交换的区域,可以把它看作是“工作层”。第二阶段当此层移动到交换床树脂层下沿时,若再运行,则进水中交换能力较小的Na+就会首先出现在水中。第三阶段,如继续运行,Na+离子全部转移至水中,当Ca2+的工作层移至树脂最下沿时,Ca2+也会出现在出水中。
所以当含有Fe3+、Ca2+、Na+的水自上而下地通过H型交换树脂时,它们在树脂层中的分布规律大体如下:
(1)被吸附离子在树脂层中的分布,是按其被树脂吸附能力的大小,自上而下依次分布,最上部是吸附能力最大的离子,最下部是吸附能力最小的离子。依据以上原理,交换后的树脂层中的离子,按自上而下的顺序排列为Fe3+、Ca2+、Mg2+、Na+和H+。
(2)各种离子被吸附能力的差异越大,则它们在树脂层中的分布就越明显(例如对化合价不同的离子)。
(3)对于交换能力差异较小的不同离子(例如化合价相同的离子),在树脂层中的分布差异并不明显,仅在同一树脂层上,表现出上、下部吸附离子含量的比例的不同。